КОЛЛОИДНЫЕ ЧАСТИЦЫ (Colloid Nanoparticles)
- В погоне за открытьем он был слишком воспален,
- И миг настал, когда нажал на крантик Кокильон.
- И закричал безумный: «Да это же коллоид!
- Не жидкость это, братцы, — коллоидальный газ!»
- Вот так, блеснув в науке, как в небе астероид,
- Простой безвестный гений безвременно угас.
- В. Высоцкий
Эффект Тиндаля

- Демонстрация эффекта Тиндаля
Взгляните на растворы, изображенные на рисунке. Внешне они кажутся практически одинаковыми — бесцветные и прозрачные. Впрочем, есть одно «но»: лазерный луч беспрепятственно проходит сквозь правый стакан, а в левом сильно рассеивается, оставляя красный след. В чем секрет?
В правом стакане — обычная вода, а вот в левом — коллоидный раствор серебра. В отличие от обычного или, как говорят химики, «истинного» раствора, коллоидный раствор содержит не молекулы или ионы растворенного вещества, а его мельчайшие частицы. Эти частицы настолько малы, что их невозможно увидеть невооруженным глазом и, более того, бывает сложно наблюдать даже с использованием новейших электронных микроскопов. Впрочем, даже мельчайшие частицы могут рассеивать свет. В физике это явление известно как «эффект Тиндаля». По этой же причине видны пылинки в солнечном луче, падающем через щель между занавесками в темную комнату. Правда, размеры и форму каждой частицы в растворе разглядеть не удастся, но все в целом они дают возможность проследить путь света.
То, что мы не сразу различили истинный раствор и коллоидный — неудивительно. Шотландский химик Томас Грэм (1805-1869), изучавший коллоидные растворы, долгое время называл их «псевдорастворами». Поскольку при выпаривании таких растворов, как правило, вместо кристаллов образуется аморфная масса, похожая на канцелярский клей, он и дал им название «коллоидных» (от греч. kolla — клей, kollodes — клейкий и eidos — вид). Кстати, каждый легко может купить концентрированную взвесь мельчайших частиц серебра в аптеке под названием «коллодий», она обладает отличными бактерицидными свойствами.
Каким же должен быть размер частиц, чтобы их раствор можно было назвать «коллоидным»? В различных учебниках коллоидными предлагается считать частицы, размер которых
составляет от 1 нм до 100 нм, от 1 нм до 200 нм, от 1 нм до 1 мкм... (рис. 1).
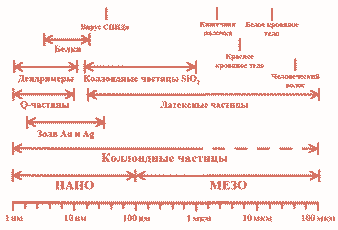
- Рис. 1. Некоторые коллоидные системы и характеристические размеры распространенных биологических объектов. На данной диаграмме диапазон размеров коллоидных частиц существенно расширен за счет полимерных (латексных) частиц, обладающих низкой плотностью. Адаптировано на основе Microscopy & Histology Catalog, Polysciences, Warrington, PA 1993-1994
Коллоидные растворы вокруг нас
Коллоидные растворы окружают нас повсюду. В огромном количестве их можно увидеть на кухне — это растворы желатина, крахмала, яичного белка и даже кисель.
 Помимо продуктов питания, коллоидные частицы могут быть найдены в таких промышленных продуктах, как лакокрасочные изделия, бумага, канцелярские принадлежности,
косметические товары, различные покрытия, фотопленки и др. Дым (например, дымовая завеса на поле боя) тоже образован коллоидными частицами, формирующими аэрозоли.
Кстати, во время боевых действий в Афганистане использовали бомбы объемного взрыва — в воздух распылялась перекись ацетона, в которую выстреливали детонаторы.
В результате это облако взрывалось, а взрывная волна (в 3-4 раза более сильная, чем при обычной детонации) уничтожала противника даже в окопах. Обычные кучерявые
облака — это тоже коллоидная система, но состоящая из взвеси капелек воды в воздухе. Все кремы, мази и эмульсии — тоже коллоиды, в которых жидкие капли (или твердые
частицы) распределены в жидкой среде.
Помимо продуктов питания, коллоидные частицы могут быть найдены в таких промышленных продуктах, как лакокрасочные изделия, бумага, канцелярские принадлежности,
косметические товары, различные покрытия, фотопленки и др. Дым (например, дымовая завеса на поле боя) тоже образован коллоидными частицами, формирующими аэрозоли.
Кстати, во время боевых действий в Афганистане использовали бомбы объемного взрыва — в воздух распылялась перекись ацетона, в которую выстреливали детонаторы.
В результате это облако взрывалось, а взрывная волна (в 3-4 раза более сильная, чем при обычной детонации) уничтожала противника даже в окопах. Обычные кучерявые
облака — это тоже коллоидная система, но состоящая из взвеси капелек воды в воздухе. Все кремы, мази и эмульсии — тоже коллоиды, в которых жидкие капли (или твердые
частицы) распределены в жидкой среде.
Тиксотропные коллоиды
Еще один пример коллоидной системы — коварные зыбучие пески, состоящие из мельчайших частиц, «перемешанных» с воздухом. Это пример тиксотропного коллоида.
Не менее важную роль коллоидные частицы играют в научных исследованиях.
Как видно из рис.1 размер различных коллоидных частиц полностью перекрывает весь нано- и мезодиапазон, что позволяет решать с их помощью самые разнообразные
методологические задачи — от калибровки электронных микроскопов
 (см.Сканирующая электронная микроскопия) до изучения биологических объектов (см. Бионанотехнологии и Оптический пинцет).
Как уже отмечалось, во многих случаях размер коллоидных частиц не превышает 100 нм,
а значит, их можно смело называть наночастицами. По этой причине многие выдающиеся нанотехнологические эксперименты современности являются современными вариациями
на тему коллоидной химии. Среди важнейших примеров коллоидных наночастиц, активно используемых в современных нанотехноло гиях, — коллоидные
частицы полупроводника А2В6, обладающие яркой люминесценцией (Квантовые точки),
магнитные коллоидные частицы (Fe/Pt, различные оксиды железа (Рис.4)) для лечения раковых заболеваний методом магнитной гипертермии (см. Наномедицина),
коллоидных частицы золота
(см.Сканирующая электронная микроскопия) до изучения биологических объектов (см. Бионанотехнологии и Оптический пинцет).
Как уже отмечалось, во многих случаях размер коллоидных частиц не превышает 100 нм,
а значит, их можно смело называть наночастицами. По этой причине многие выдающиеся нанотехнологические эксперименты современности являются современными вариациями
на тему коллоидной химии. Среди важнейших примеров коллоидных наночастиц, активно используемых в современных нанотехноло гиях, — коллоидные
частицы полупроводника А2В6, обладающие яркой люминесценцией (Квантовые точки),
магнитные коллоидные частицы (Fe/Pt, различные оксиды железа (Рис.4)) для лечения раковых заболеваний методом магнитной гипертермии (см. Наномедицина),
коллоидных частицы золота
 (см. Плазмонный резонанс) медицинских применений, сферические коллоидные частицы на основе полистирола оксида кремния для получения фотонных
кристаллов и двумерных упорядоченных структур (см. Фотонные кристаллы, Самоорганизованных системы и Наносферная литография) и многие другие.
(см. Плазмонный резонанс) медицинских применений, сферические коллоидные частицы на основе полистирола оксида кремния для получения фотонных
кристаллов и двумерных упорядоченных структур (см. Фотонные кристаллы, Самоорганизованных системы и Наносферная литография) и многие другие.
- Рис. 4. Структура Green Rust 1, сформировавшаяся на поверхности стали при ее контакте с водным раствором AgNO3


 Рубрика "Это интересно" освещает инетресные и занимательные факты развития нанотехнологий «Мир НАНО.
Рубрика "Это интересно" освещает инетресные и занимательные факты развития нанотехнологий «Мир НАНО.